应用深度学习模型成功地在头颅CTA上检测到临床上有意义的颅内动脉瘤,这表明人工智能辅助诊断模型可以提高临床医师的工作效率,并提供可靠和准确的判断,从而优化患者健康服务。
————摘自文章章节
【Ref:Park A,et al. JAMA Network Open. 2019;2(6):e195600. doi: 10.1001/jamanetworkopen.2019.5600.】
研究背景
人群中未破裂颅内动脉瘤发生率1%-7%,计算机断层扫描血管造影(CTA)是目前颅内动脉瘤诊断和术前规划的主要成像方式,而对神经放射学家来说大量的阅片,占用时间很长。目前卷积神经网络在一系列医学图像分析中表现出色,因此开发一个深度学习模型来识别CTA中有临床意义的动脉瘤,可能为放射科医生、神经外科医生和其他临床医生提供一个适用的诊断工具。本研究开发了一个深度学习模型来自动检测CTA上的颅内动脉瘤,并对感兴趣区域进行自动分段,以帮助临床医生解释检查结果。同时比较有和无人工智能辅助下的临床医生工作效率,包括敏感性、特异性、准确性、时间长短和评判者之间的一致性。
研究方法
我们回顾性研究了2003年1月3日至2017年5月31日在斯坦福大学医学中心进行的头部或头颈部共9455例连续CTA检查报告。由一名具有12年经验的神经放射学家检查并排除:实质性脑出血、蛛网膜下腔出血、创伤后或感染性假性动脉瘤、动静脉畸形、缺血性中风、非特异性或慢性血管病变,如颅内动脉粥样硬化或其他血管病变,以及动脉瘤夹、弹簧圈、导管或其他外科手术植入物等。检查报告主要包括未破裂动脉瘤(>3mm)。测试集中所有检查标准由一位经过认证的、具有12年经验的神经放射学家确定。首先是通过原始放射学报告确定动脉瘤的存在,同时对CTA检查原始数据进行双重审查。如果必要可通过诊断性脑血管造影进一步确认动脉瘤。放射科医师首先确定每个动脉瘤的位置,同时使用开源注释软件ITK-SNAP,在每张片子上手动标注所识别的动脉瘤。最后建立一种名为HeadXNet的三维CNN模型,用于从CTA数据中自动分割颅内动脉瘤。
研究设计
这是一项诊断准确性研究,比较HeadXNet模型是否可提高的临床医生的诊断能力。临床医生对原始报告、临床病史和随访影像均不知情。采用交叉设计,将8名临床医生随机平均分为两组,在每一组中均安排无模型和有模型辅助诊断,中间有2周洗脱期,而检查次序相反。
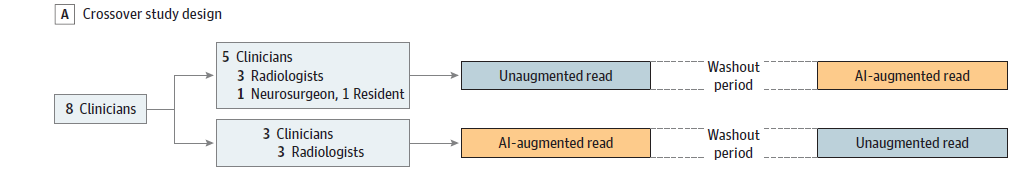
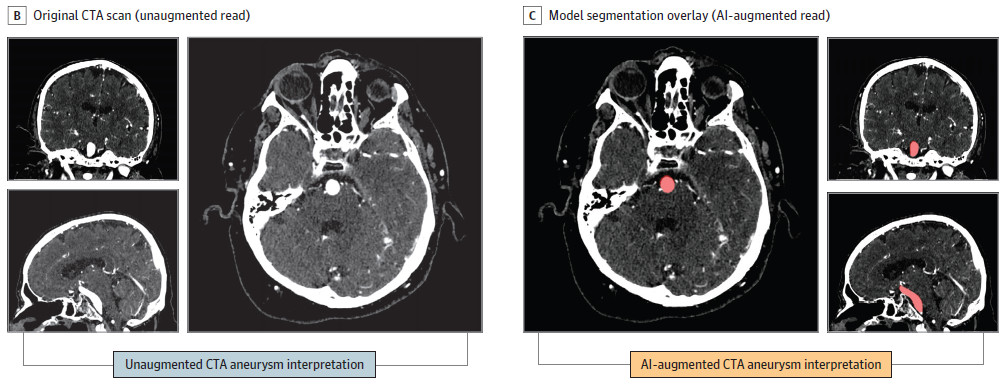
临床医生依据动脉瘤直径大于3mm来确定是否存在动脉瘤。临床医生在一个数据录入软件应用程序中输入标签。为了确保所有临床医生都熟悉的图像显示界面,而在有模型辅助情况下,如果模型预测动脉瘤概率大于0.5,临床医生可以看到轴向、矢状和冠状序列上都有一个半透明的红色覆盖(如上图),临床医生可以在加载检查时立即访问感兴趣区,再根据这个进行判读。
研究结果
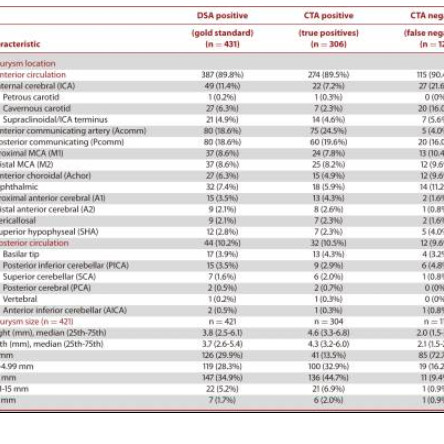
9455例次CTA检查,发现818例次动脉瘤。这些测试被分为训练集、开发集和测试集,分别用于训练模型、选择最佳模型和评估所选择的模型。数据集包含662例患者的818项检查,其中328项CTA检查(40.1%)中至少有1个颅内动脉瘤,490项检查(59.9%)中没有颅内动脉瘤。其中3mm~7mm动脉瘤148例,7mm-12mm动脉瘤108例,12mm-24mm动脉瘤61例,24mm及以上动脉瘤11例。动脉瘤主要位于颈内动脉、大脑中动脉、颈内动脉海绵窦段、基底动脉顶端、前交通动脉和后交通动脉。
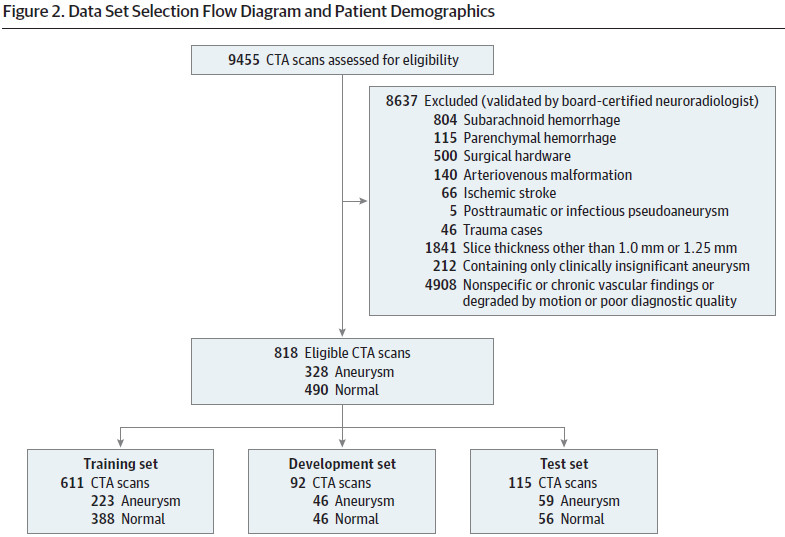
采用分层随机抽样的方法,形成包括50%动脉瘤检查和50%正常检查在内的开发集和测试集;其余检查均为训练组,其中动脉瘤检查占36.5%。用于训练模型的训练集有611例次检查(494名病人,平均年龄55.8岁,其中223例动脉瘤),用于开发集有92项检查(86名病人,平均年龄61.6岁,其中46例动脉瘤);用于测试集中有115项检查(82名病人,平均年龄57.8岁,其中59例动脉瘤)(图2)。
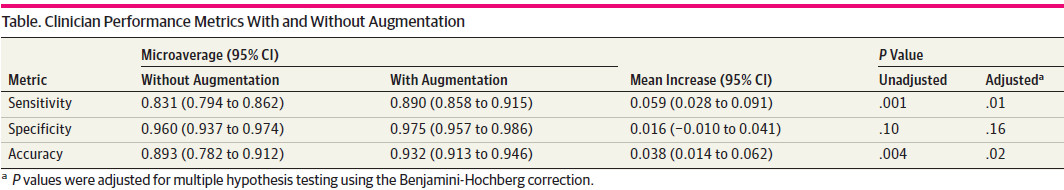
临床医师在未使用模型的情况下,灵敏度为0.831,特异性为0.960,准确率为0.893;在使用模型的情况下,临床医生的诊断灵敏度为0.890,特异性为0.975,准确率为0.932。(如表1)。
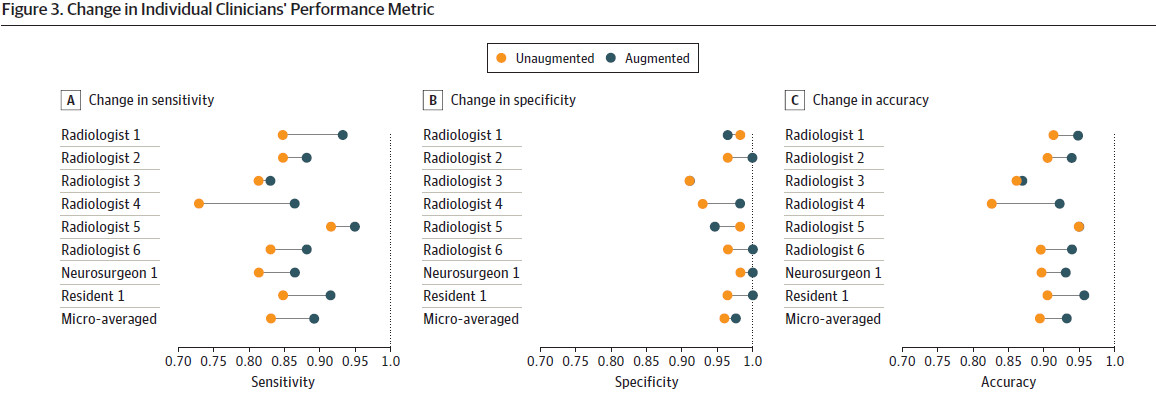
上述水平线描述了每个临床医生在有或没有模型辅助情况下各项诊断性能指标的变化。橙色点表示没有模型的性能,蓝色点表示有模型辅助的性能。在有模型的情况下,临床医师平均诊断时间较无模型辅助没有明显的下降((5.71秒对18.63秒),该模型处理检测结果并输出分割图平均耗时7.58秒。对比有模型和无模型,临床医生之间的一致性显著增加0.060 (P= 0.05)。
讨论
在本研究采用交叉研究设计,研究HeadXNet模型是否提高临床医生CTA检查诊断脑动脉瘤的能力,结果表明在使用HeadXNet模型的情况下,临床医生的敏感性、准确性和一致性显著提高,而特异性和诊断时间上无统计学差异。
研究表明应用CTA检查诊断动脉瘤,判读者的一致性是高度可变的,从0.37到0.85不等,判读者的水平取决于动脉瘤的大小和放射科医生的经验。该模型可自动检测动脉瘤,显著提高临床医生CTA检查诊断的敏感度和准确度,显著提高判读者的一致性,从0.799提高到0.859。这意味着具有不同经验水平和不同专业的临床医生使用该模型后可以得到更准确和更一致的结果。同时它也可用来优化工作流程,缩短治疗时间,得到更好的结果。
但本文有一定局限性。首先由于本研究只纳入未破裂动脉瘤,未纳入破裂动脉瘤、介入栓塞后或手术夹闭术后复发的动脉瘤或动静脉畸形相关的破裂动脉瘤;其次,由于排除了包含手术植入物的CTA检查资料,因此该模型在这种复杂情况下的性能是未知的。此外,本研究是针对一家医疗机构的CTA数据进行的,当应用于其他机构的数据时(不同机器、不同的扫描模式与扫描厚度),可能会对结果产生偏差。
研究结论
建立的HeadXNet深度学习模型可成功地检测出CTA上临床意义显著的颅内动脉瘤,这表明人工智能辅助诊断模型可显著提高临床医生诊断颅内动脉瘤的敏感性、准确性和临床医生的一致性。