今天为大家分享的是由吉林大学第一医院侯坤医师翻译,苏州大学附属第二医院朱卿教授审校的:后循环动脉瘤:夹闭或栓塞?,欢迎观看、阅读!
显微手术和血管内治疗都是治疗后循环动脉瘤安全、有效的方式;但根据两种治疗方式的不同风险,特别是位于穿支丰富区域以及脑干前方时,治疗这些特定的后循环动脉瘤具有明显的适合治疗方式。
虽然大部分后循环动脉瘤为囊状动脉瘤,但该区域夹层假性动脉瘤和梭形动脉瘤的发生率较高。
在制定后循环动脉瘤的治疗计划时,要考虑病变可及性、动脉瘤与穿支血管及后床突的解剖关系、双抗治疗的必要性/安全性(尤其在破裂动脉瘤合并脑积水的患者)。
后循环动脉瘤包括椎动脉(VA)、椎基底(VB)交界、基底动脉分叉、小脑后下动脉(PICA)、小脑前下动脉(AICA)、小脑上动脉(SCA)和大脑后动脉(PCA)动脉瘤。与前循环动脉瘤不同,这些动脉瘤因位置深在而入路困难,形态更复杂。
由于后循环动脉瘤起源于脑干前方,供应非常重要的区域,发生并发症往往是灾难性的,因而治疗起来比前循环动脉瘤更困难。
虽然血管内治疗和显微手术治疗都有潜在的神经系统并发症,但目前的治疗方式已从显微手术向血管内治疗过渡。在过去10年间,经验积累和研究的增多使得这一趋势更加明显,比如国际动脉瘤性蛛网膜下腔出血试验(ISAT)和国际未破裂颅内动脉瘤研究(ISUIA),结果均显示后循环动脉瘤显微手术的并发症发生率高于血管内治疗。
尽管如此,不加区分地套用治疗原则仍是不明智的。所有动脉瘤的治疗都应由包含高级显微手术和血管内治疗专家在内的多学科团队进行评估,以根据不同动脉瘤和患者的特征来决定最终的治疗计划。
本章节将重点讨论后循环动脉瘤选择显微手术还是血管内治疗的细节问题。许多概念已在“前循环动脉瘤:夹闭或栓塞“章节中进行了探讨。
基底动脉分叉部动脉瘤:显微夹闭病例
基底动脉分叉部动脉瘤的显微手术在技术上颇具挑战性,因为这类动脉瘤的手术可及性相对较差,操作可带来较高的丘脑穿支梗塞风险。有3个解剖间隙可到达基底动脉分叉部,包括视神经-颈内动脉、颈内动脉-动眼神经和不常用的颈内动脉上三角。手术的风险在于未能充分确认丘脑穿支动脉以及未能做到理想的近端血管控制。
另外,瘤顶的指向、基底动脉分叉部与后床突的关系也会影响手术的可及性。指向上方和后方的动脉瘤可遮挡远端瘤颈后方的穿支动脉,而指向前方的动脉瘤可遮挡对侧SCA和PCA。对于指向前方的动脉瘤,穿支血管从瘤顶发出,分离并保护穿支动脉比较容易。
另一方面,指向后方的动脉瘤将穿支动脉压向瘤颈背侧,使得这类动脉瘤的手术异常困难。
手术的可及性取决于基底动脉分叉部与后床突的垂直关系。高位基底动脉分叉部被ICA遮挡,需进行头侧的神经血管分离才能观察到瘤颈,但从近端控制载瘤动脉比较容易。穿支动脉的起源也更靠下,便于从瘤颈分离。
后床突可遮挡低位基底动脉分叉部,阻碍对近端载瘤动脉的确切控制。并且在这种血管条件下,穿支血管的走行更加垂直,阻碍其解剖和分离。考虑基底动脉分叉部与天幕缘、后床突的解剖关系,颞下入路更有优势。
PCA(P1)近端动脉瘤与SCA动脉瘤在手术显露方面类似。均为侧方起源,经侧裂入路易于显露,但与SCA动脉瘤不同,其对丘脑穿支动脉(发自PCoA或P1段,常与瘤顶或瘤颈黏连)的手术视角是呈切线方向的。
PCA远段动脉瘤暴露困难,应进行个体化评估,所幸比较罕见。虽然可经颞下入路到达PCA远端动脉瘤,但由于术野可视性差和颞叶牵拉较重,并发症发生率高。
病例1
女,43岁,基底动脉分叉部动脉瘤破裂引起SAH,Hunt-&Hess Ⅳ级。与血管内治疗团队讨论后,由于动脉瘤颈宽,行显微手术夹闭。
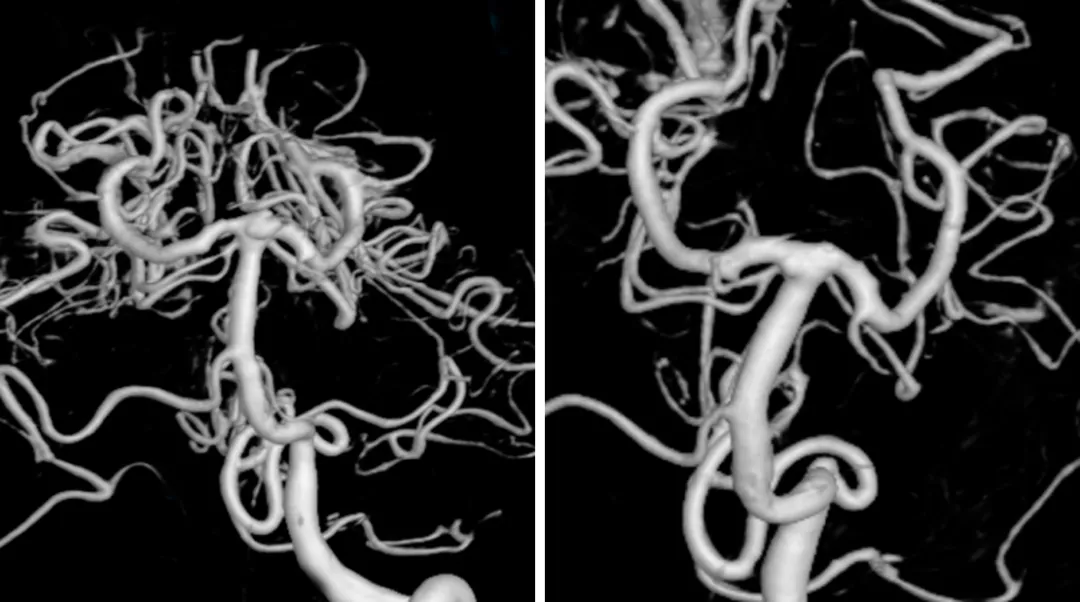
图1. DSA三维重建后显示指向前方的高位、宽颈基底动脉分叉部动脉瘤 (左)。术后影像显示动脉瘤完全夹闭(右)。
基底动脉尖动脉瘤:血管内治疗病例
由于显露脚间池的安全性有限,以及操作对丘脑穿支动脉存在风险,这类动脉瘤更适合行血管内治疗。
当然,血管内治疗也不是万全之策。基底动脉分叉部动脉瘤通常宽颈,累及一侧或双侧P1段。如果指向后方或正好低于鞍背,血管内治疗明显优于手术夹闭。虽然血流导向装置已成功应用于一些患者中,但应避免用于基底动脉分叉部穿支血管丰富的患者。球囊或支架辅助栓塞是有效、安全的。
最佳的支架释放方式应当是通过PCoA自一侧P1到达对侧P1,这种方式可重建基底动脉分叉部,并有利于栓塞动脉瘤。不幸的是,许多患者的PCoA条件并不匀许这么做。
其他支架释放方式包括从基底动脉到一侧P1(一侧式)、Y型支架(从BA到双侧P1),T型支架(通过PCoA从一侧P1到另一侧P1)。从技术角度讲,一侧式是最直接的方法,但并不能充分缩小瘤颈以保护未植入支架的P1段。Y型和T型支架更能保护双侧P1,但操作更复杂,对经验和技术的要求高。球囊辅助栓塞技术可将球囊自P1到基底动脉或经PCoA从P1到P1。
基底动脉主干动脉瘤通常是夹层假性动脉瘤或基底动脉开窗动脉瘤。两种类型均可通过支架重建行血管内治疗。由于基底动脉干富含穿支血管的特点,血流导向装置只能留待特殊情况使用。开窗处动脉瘤行弹簧圈栓塞,而夹层假性动脉瘤采用双支架(即支架内套支架)技术是一种合理的选择。
病例2
男,75岁,因TIA起病,意外发现基底动脉分叉部动脉瘤。以支架辅助弹簧圈栓塞。高龄患者行血管内治疗获益最多。
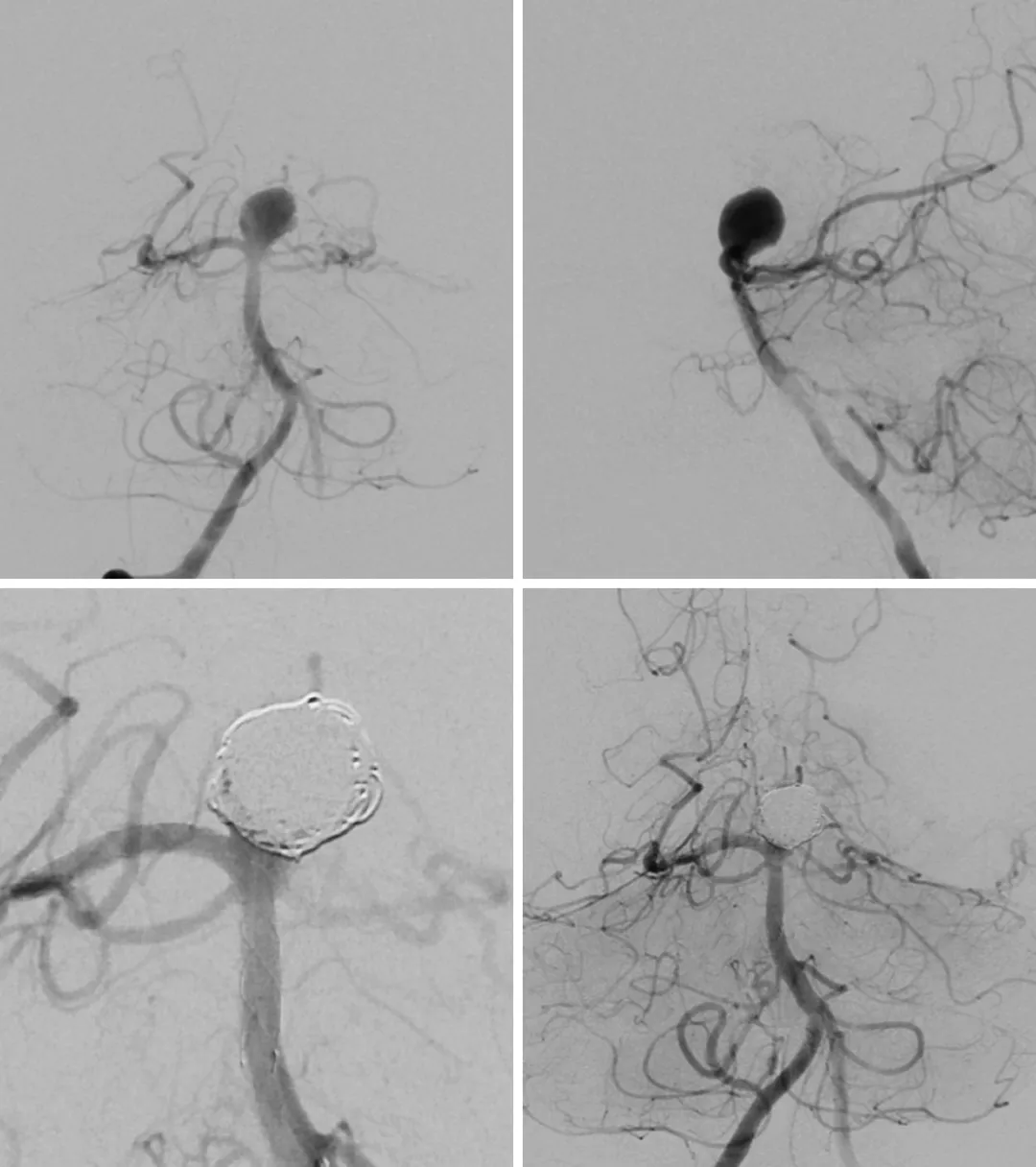
图2. 前后位和侧位血管造影(上排)显示基底动脉分叉部动脉瘤。术后血管造影(下排)显示动脉瘤Raymond 3级栓塞。
病例3
女,70岁,因基底动脉中段侧壁动脉瘤来诊。既往有大脑中动脉卒中史。行支架辅助弹簧圈栓塞。
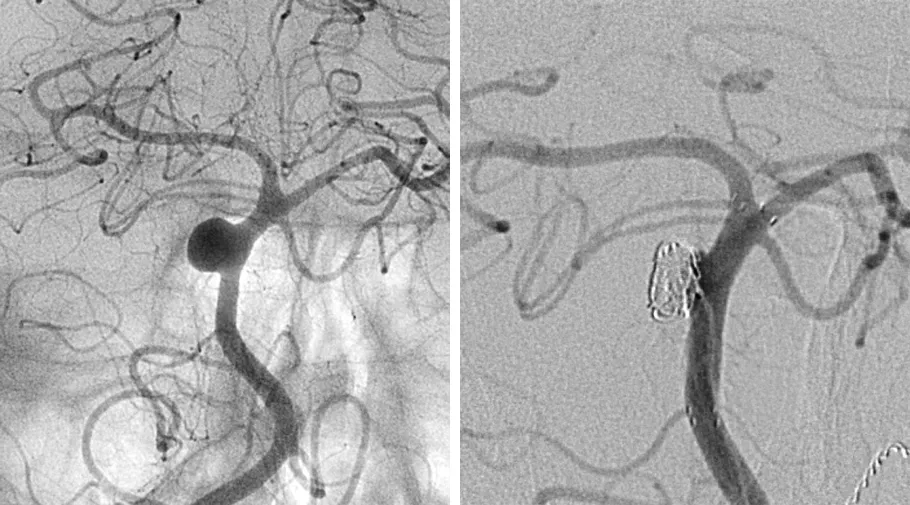
图3. 后循环DSA显示基底动脉夹层动脉瘤。术后血管造影显示Raymond 3级栓塞。此类型动脉瘤尚无较好的显微手术方法。
PICA动脉瘤:显微夹闭病例
显微手术仍是PICA和远段AICA动脉瘤的重要治疗方法。PICA和AICA管径较细,常发自动脉瘤颈部,血管内治疗具有一定危险性。
这些病灶可较容易地通过枕下外侧入路或扩大乙状窦后入路到达,尤其是位于远端血管者,分支血管少,最小的解剖操作即能容易进行近端控制。
虽然,PICA近段动脉瘤在技术上更具挑战性,但仍可安全地分离并保护后组颅神经和横行的穿支血管。当载瘤动脉无法保留而需行血流重建时,仍能很好地耐受临时血流阻断。
病例4
女,39岁,左侧PICA起始处动脉瘤破裂致SAH,Hunt-Hess Ⅱ级。经左侧枕下外侧入路行动脉瘤夹闭术。术后血管造影证实动脉瘤完全夹闭。
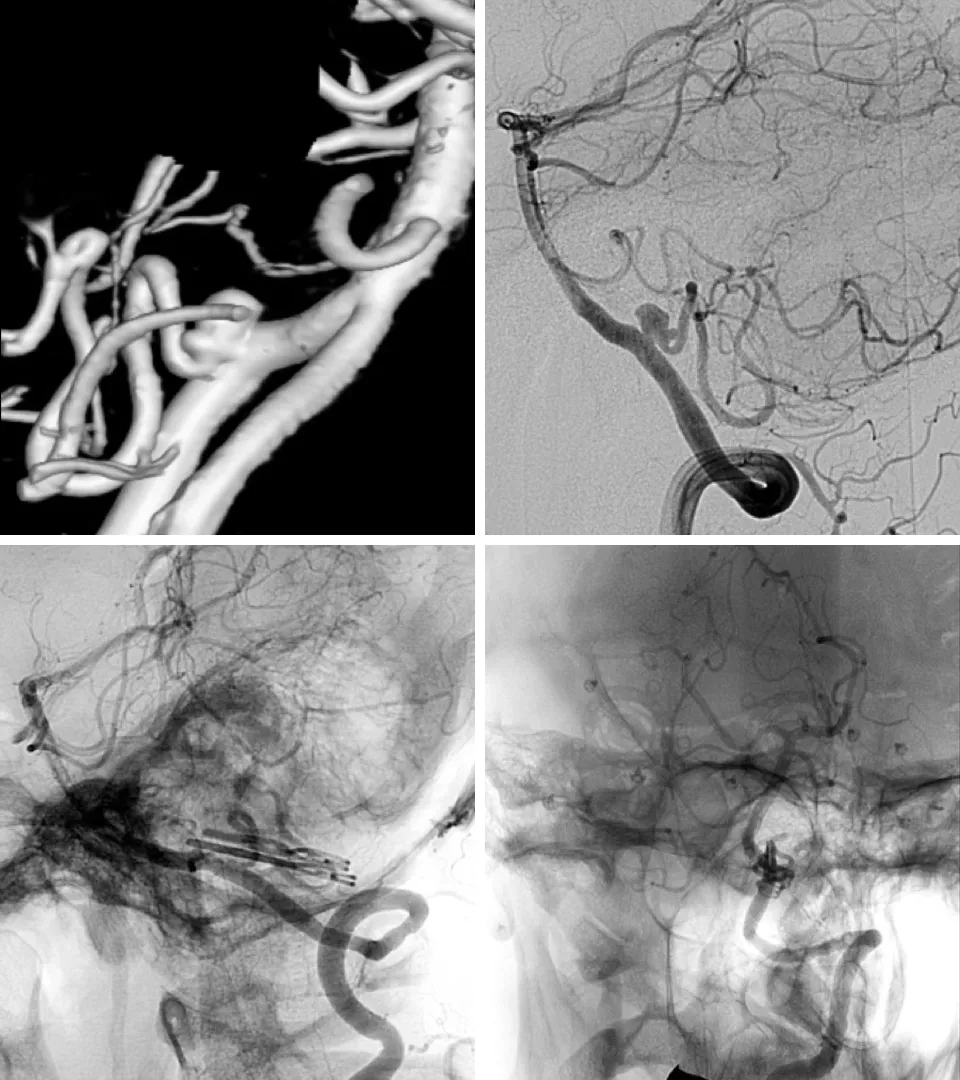
图4. 血管造影显示PICA起始处动脉瘤(上排)。PICA管径细且起源于动脉瘤颈部。术后血管造影证实以两枚动脉瘤夹完全夹闭动脉瘤(下排)。
病例5
男,70岁,PICA动脉瘤破裂。由于PICA动脉迂曲,血管内治疗未成功。遂行显微手术完全夹闭动脉瘤。
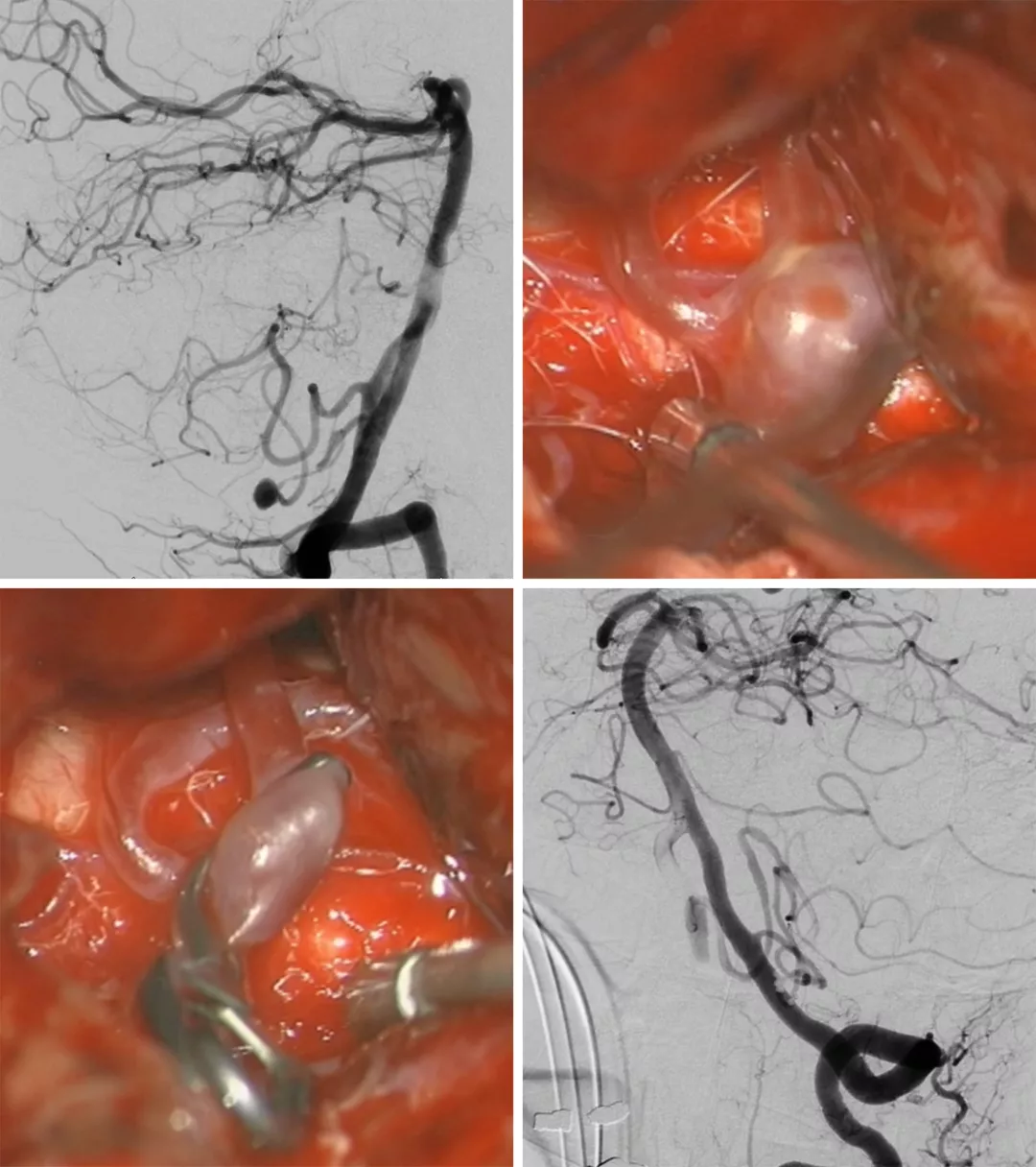
图5. PICA远段动脉瘤(左上),血管内治疗未成功。动脉瘤夹(右上、左下)成功将宽颈动脉瘤夹闭,保留PICA(右下)。
PICA动脉瘤:弹簧圈栓塞病例
PICA动脉瘤包括PICA起始处动脉瘤和PICA远段动脉瘤。椎动脉夹层动脉瘤和PICA起始处动脉瘤有明显的概念重叠,但本章节仅讨论PICA起始处的囊状动脉瘤。
PICA起始处动脉瘤可起自VA或PICA。PICA常发自动脉瘤颈。显微手术更容易保留PICA起始处;但当PICA起始处能容易地通过血管内技术保留时,弹簧圈栓塞/支架植入/血流导向装置置入是一种持久、安全和耐受性良好的治疗方式。
VA动脉瘤最常累及PICA起始处。不累及PICA的VA动脉瘤通常是穿过硬脑膜自V4向远端发展的夹层假性动脉瘤。放置或不放置弹簧圈下行双支架置入技术(支架内套支架)可用于处理此类动脉瘤。该区域通常无穿支动脉,血流导向装置已安全、有效地用于治疗VA动脉瘤。
PICA远段动脉瘤通常更容易行夹闭术。另一个需要考虑的问题是PICA、SCA和AICA的血供重叠,在某些患者即使牺牲PICA也不会导致不良后果。
病例6
女,52岁,基底动脉分叉部和PICA动脉瘤。先施行单纯弹簧圈栓塞治疗两个动脉瘤。PICA动脉瘤需球囊辅助固定微导管以防止被踢出。
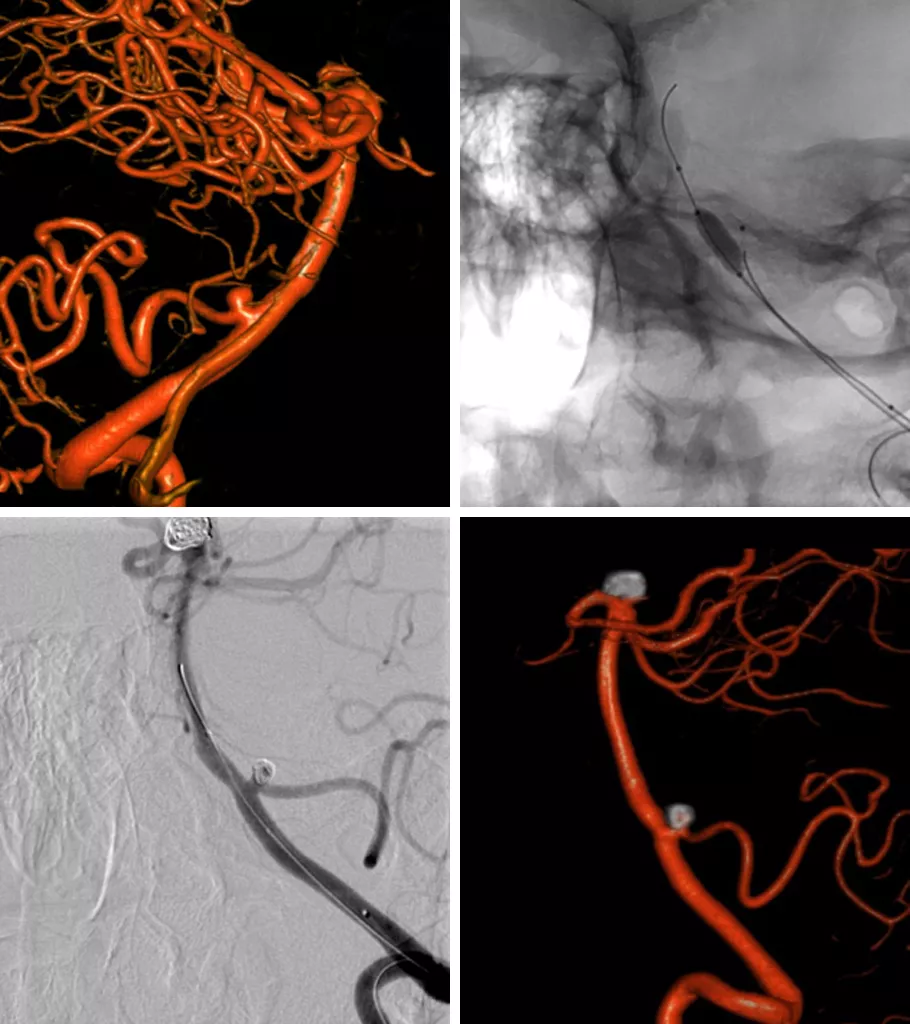
图6. 三维重建显示,PICA动脉瘤较小且宽颈,单纯弹簧圈栓塞(左上)。由于工作角度不理想且动脉瘤较小,为避免微导管脱出,球囊在椎动脉处固定微导管(右上)。最终获得稳定的弹簧圈栓塞动脉瘤(下排)。
病例7
男,56岁,因头痛行检查时发现PICA起始处夹层动脉瘤。用密网支架行血管内治疗。术后,血管造影显示与血管壁贴合良好,造影剂在瘤顶滞留,瘤囊不完全充盈,PICA显影良好。
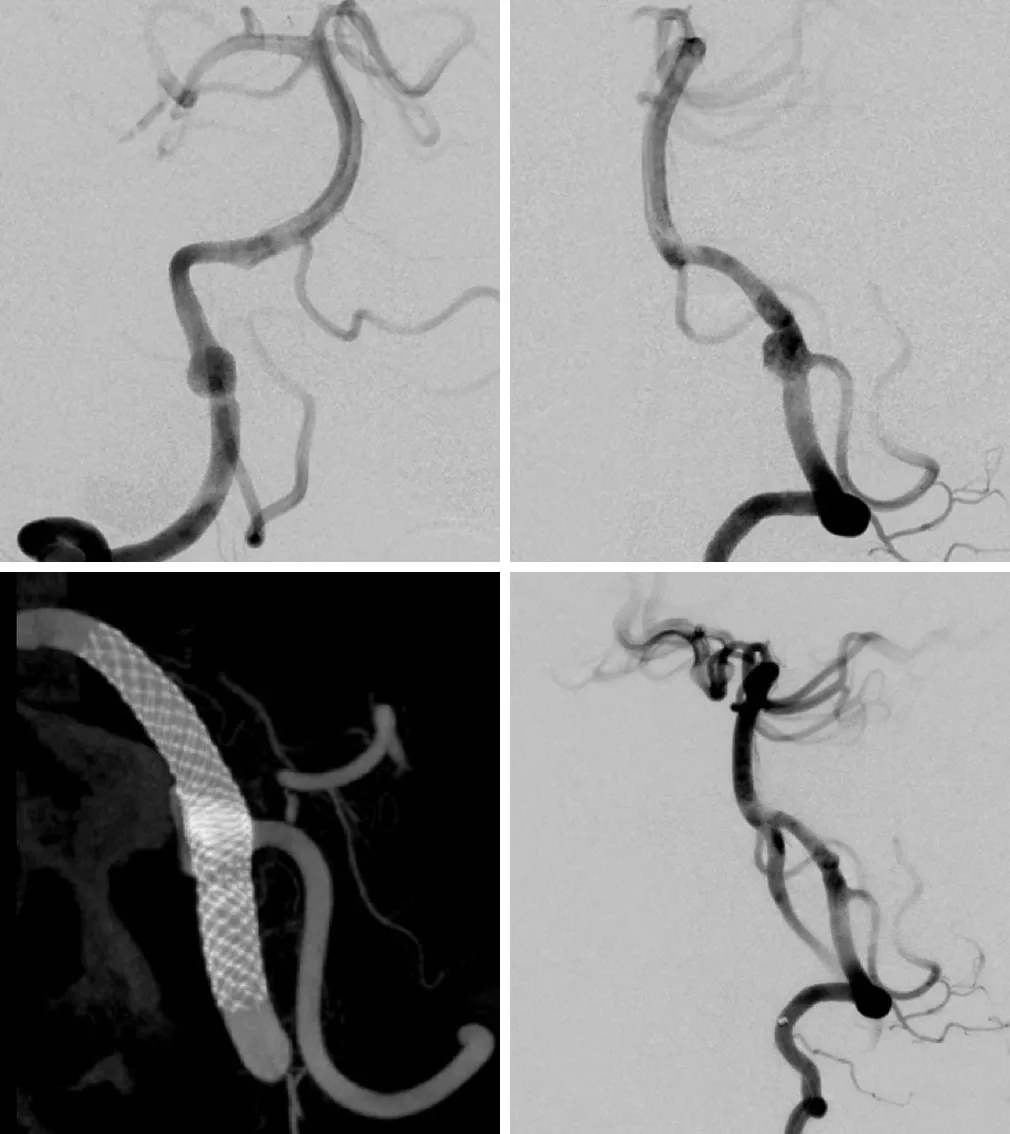
图7. 右侧VA血管造影显示PICA起始处夹层动脉瘤(上排)。DynaCT三维重建显示支架在动脉瘤部位与血管壁贴合良好(左下)。术后血管造影显示动脉瘤不显影(右下)。
SCA动脉瘤:显微夹闭病例
由于瘤颈在解剖上很少有脑干穿支发出,SCA动脉瘤比基底动脉分叉部动脉瘤更适合显微手术夹闭。这些重要的丘脑穿支既不发自PCA起始部下方,也不发自SCA起始部上方。而且,SCA动脉瘤指向外侧,经侧裂入路视野良好。
这些独特的解剖学优势决定了SCA动脉瘤的瘤颈容易安全地暴露,无需广范分离或冒穿支梗塞的风险。虽然没有高位的SCA动脉瘤,但低位SCA动脉瘤更难在手术中暴露,可能需要磨除后床突或鞍背。总之,SCA动脉瘤容易达到,穿支动脉风险小。
病例8
男,55岁,意外发现基底动脉分叉部动脉瘤和左侧SCA动脉瘤。采取额眶颧开颅夹闭SCA动脉瘤,然后行支架辅助栓塞基底动脉分叉部动脉瘤。
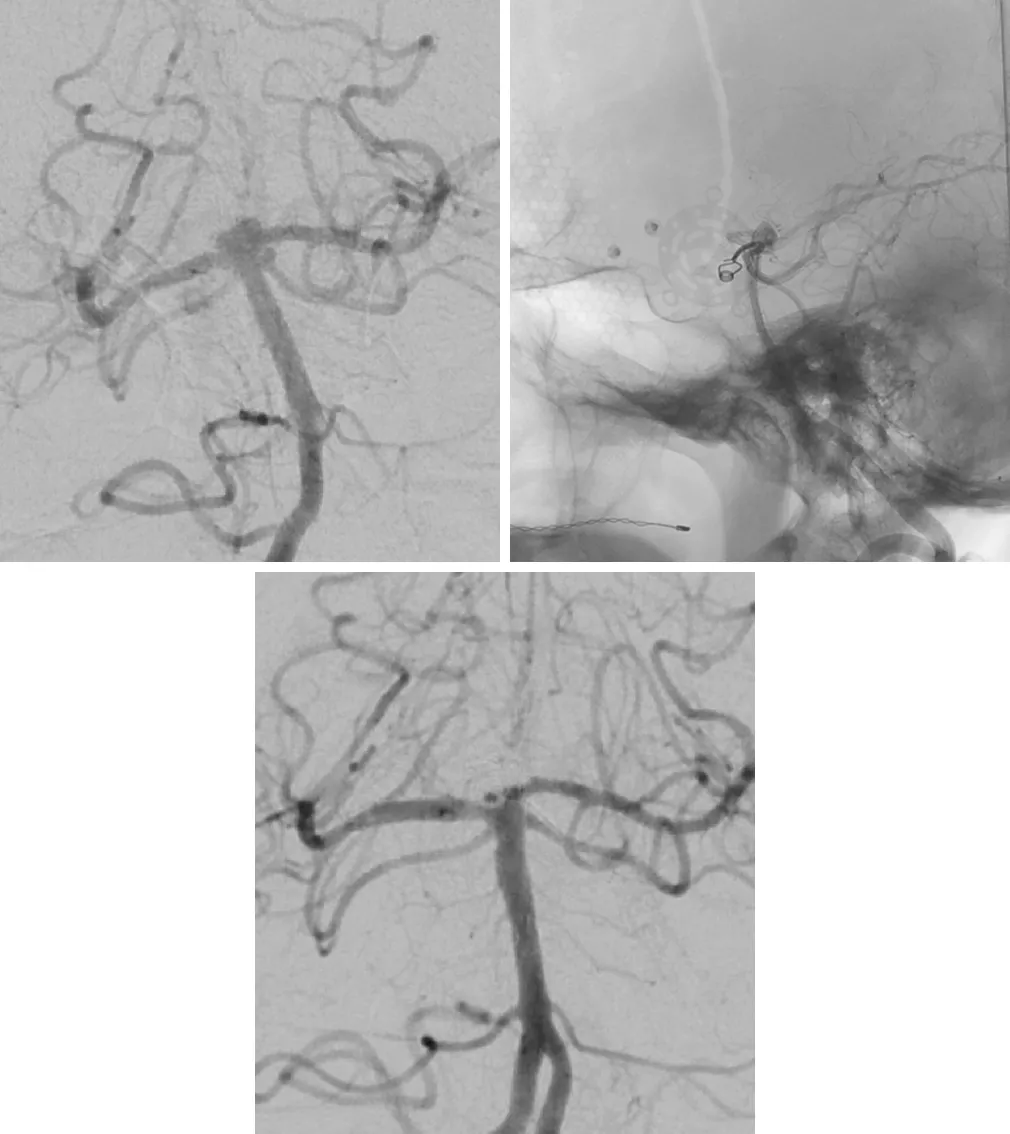
图8. 血管造影显示基底动脉分叉部和左侧SCA动脉瘤(左上)。右侧骨窗像显示高位基底动脉分叉部,在行SCA动脉瘤夹闭(右上)时不能同时夹闭。术后血管造影显示两个动脉瘤均成功处理(底部)。
SCA动脉瘤:血管内治疗病例
多数SCA动脉瘤较小,SCA与基底动脉管径相差大,导致无论是单纯弹簧圈栓塞还是球囊或支架辅助栓塞均困难。AICA动脉瘤也是如此,如果手术能够显露,夹闭是更有效的选择。另外,对于老年且合并其他健康问题的患者,保护性次全栓塞也是合理的选择。
病例9
女,70岁,以TIA起病,检查发现左侧SCA动脉瘤。行弹簧圈栓塞治疗。2年后MRA显示无复发。
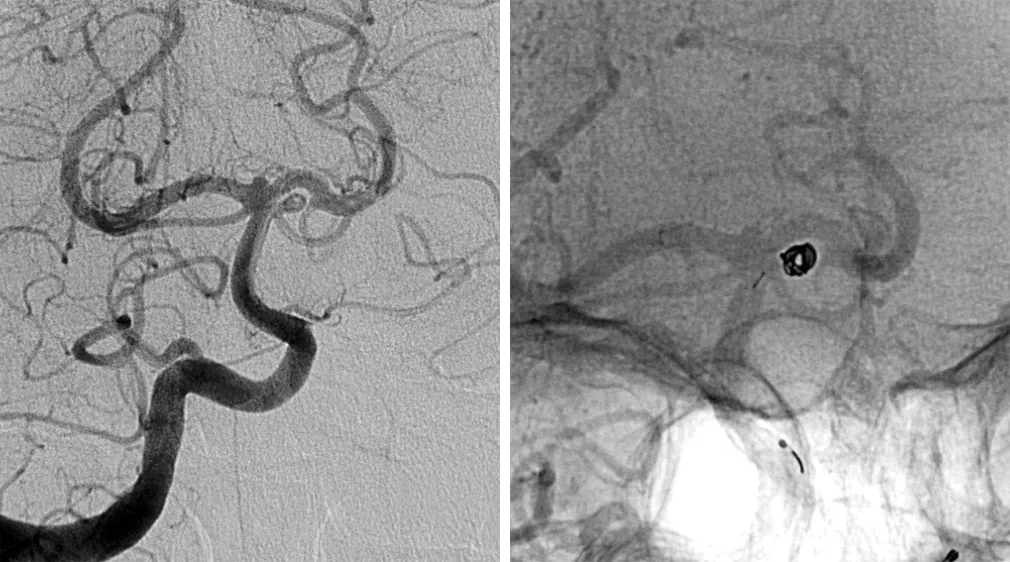
图9. 显示左侧SCA动脉瘤(左)。栓塞后血管造影显示动脉瘤不显影,正常血管结构保护良好(右)。
后循环夹层、巨大或复杂形态动脉瘤
复杂动脉瘤有多种类型,包括巨大、多叶、夹层、蛇形、梭形和宽颈动脉瘤。动脉瘤宽颈、瘤内血栓形成、位于动脉远段或有血管发出时,血管内治疗困难,因为通常不能完全栓塞,需多次治疗。
另一方面,手术也极具挑战性且充满风险;但手术可以显露且能有效控制近端者仍应选择手术治疗。PICA动脉瘤就是如此,通常比较复杂,手术可到达也能处理。
椎动脉动脉瘤通常是夹层动脉瘤,无瘤颈可供夹闭。这类病灶容易发生术中破裂,不容易控制血流。
手术处理后循环系统的大型、夹层或梭形动脉瘤通常需要高创伤性的辅助措施,包括低温停循环、广泛的颅底暴露、过久的血流阻断。这些因素导致手术治疗的效果不如血管内治疗。但对于血栓性动脉瘤压迫脑干导致病情迅速恶化的患者,手术仍有一席之地。
某些夹层或梭形动脉瘤可选择血流导向装置。血流导向装置在穿支动脉丰富的区域可引起严重并发症,所以介入医生在穿支丰富的基底动脉、基底动脉分叉部和椎基底交界区应避免使用血流导向装置。在该区域使用血流导向装置的确切危险性,还远没有定论。
病例10
男,62岁,因椎基底动脉交界区(VBJ)2.5cm的巨大动脉瘤而首先行右侧椎动脉(VA)弹簧圈闭塞。此动脉瘤逐渐增大,导致脑干压迫症状。随后,在低温停循环下行夹闭重建。患者的mRS评分在6个月内从5分到3分,1年后为2分。
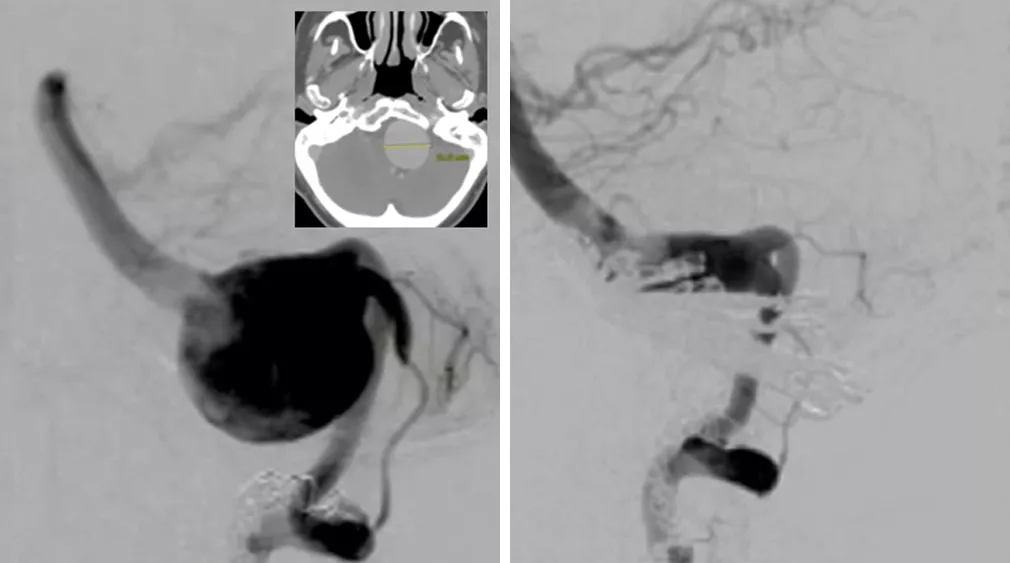
图10. 轴位CT(插入图)显示巨大椎基底交界动脉瘤导致脑干压迫(左)。瘤体进行减压并夹闭重建(右)。
DOI: https://doi.org/10.18791/nsatlas.v3.ch01.2.2
相关链接




