Bilateral parafalcine meningioma_Atlas
Giant bilateral anterior parafalcine meningioma-Transfalcine-Atlas
Posterior parafalcine meningioma_Atlas
今天为大家分享的是由上海市第一人民医院昆山分院马鹏医师翻译,《神外资讯》常务编辑、海军军医大学附属长征医院神经外科徐涛医师审校的:镰旁脑膜瘤手术策略与技巧(Parafalcine Meningioma),欢迎观看、阅读。

图1. Cushing和他的同事(Dr.Gaston Decoppet)在讨论一位颅内肿瘤复发患者的病情。
镰旁脑膜瘤起源于大脑镰,约占颅内脑膜瘤的8.5%。与矢状窦旁脑膜瘤不同的是,镰旁脑膜瘤可完全被脑皮质覆盖,可突破大脑镰并常常呈双侧生长。与矢状窦旁脑膜瘤类似的是二者均最多见于上矢状窦中1/3(冠状缝与人字缝之间)。
诊断
和矢状窦旁脑膜瘤类似,镰旁脑膜瘤的临床表现主要取决于其沿大脑镰生长的部位。中央沟附近的肿瘤可引起癫痫发作或对侧肢体感觉及运动障碍。如果肿瘤累及优势半球辅助运动区(SMA)可引起语言障碍。
大脑镰前1/3肿瘤体积可以长到很大并引起认知障碍、头痛、视物模糊或视乳头水肿。大脑镰后1/3肿瘤可引起视觉障碍,如同向偏盲或者幻觉。镰旁脑膜瘤偶尔也会引起脑内、硬膜下或蛛网膜下出血。
罕见情况下肿瘤可仅引起单一的对侧下肢无力。注意不要与脊髓神经根受压引起的功能障碍相混淆。上运动神经元体征(可能很细微)以及肌无力分布范围(与个别神经根受压引起的肌群受累无关)可用于两者的临床鉴别。
评估
磁共振(MRI)可见双侧半球间以大脑镰为基底伴脑膜尾征的轴外肿瘤。T2加权像可用于评估大脑前动脉末端及其分支的分布。脑实质水肿意味着软脑膜受侵犯,与术后神经功能障碍相关。
MR或CT静脉造影可用于评估上矢状窦受侵犯或闭塞程度以及明确大的矢状窦旁桥静脉及其属支位置。这些静脉的位置可用于指导手术入路,以确保在大脑半球间获得足够的手术空间抵达肿瘤。体积较大的肿瘤经常包绕胼周动脉及胼缘动脉,术前应行CTA鉴别这些被包绕或推移的重要血管。
需要与镰旁脑膜瘤鉴别的病变主要有转移瘤、骨软骨瘤及软骨肉瘤。

图2. 不同体积的镰旁脑膜瘤。CTA显示胼周动脉及胼缘动脉被体积巨大的肿瘤包绕。
手术适应症
症状进行性加重的患者应行手术治疗。肿瘤体积较小的,无症状的患者可定期影像学检查,随访。重要桥静脉及静脉窦遭部分侵犯的肿瘤可予次全切除,残余瘤体予放射治疗。
术前注意事项
术前腰大池引流有助于松弛脑组织,最大程度减少术中对脑组织的牵拉(尤其对于体积较大的肿瘤)。在纵裂入路显露镰旁脑膜瘤的过程中不进入充满脑脊液的脑池,因而腰大池引流显得尤为重要。选择性脑皮质切除行内减压更是不必要的。对于造成明显占位效应和中线移位的巨大脑膜瘤,笔者从未遇到过因术中腰大池引流而导致小脑幕切迹疝的情况。硬脑膜打开后即可行腰大池引流,逐次缓慢释放CSF10ml直至脑组织松弛。
由于在手术初始阶段即可阻断大脑镰层面的肿瘤血供,因此笔者并不提倡术前行肿瘤血管内栓塞。
随着放射医学的发展,笔者也在不断更新对脑膜瘤手术的理念。考虑到手术要以病人安全为核心,对于侵犯重要动静脉的脑膜瘤,目前手术目标更倾向于次全切除,而不是激进的完全切除。影像学随访发现残余肿瘤生长可行放射治疗。
镰幕交界处脑膜瘤经常会挤压或包绕间脑周围静脉(如Galen静脉及Rosenthal静脉系)及直窦。由于该区域血管很重要,术前DSA有助于了解该区域血管分布情况。次全切除有助于确保重要脑血管结构不受损伤。
镰旁脑膜瘤切除技巧
关于肿瘤入路的一些细节问题请参阅经纵裂入路或顶部开颅术(原文请扫下方二维码)章节。对于镰旁脑膜瘤开颅过程中有一些特别的注意事项。
和矢状窦旁脑膜瘤不同,大部分镰旁脑膜瘤采用直切口即可行手术切除。切口应跨中线以便暴露上矢状窦并在硬膜打开后通过大脑镰浅部的牵引缝线将静脉窦向侧方移动。头侧位可利用重力牵引脑组织从而获得更大的操作空间。体积巨大、双侧生长的镰旁脑膜瘤可通过单侧直切口开颅经大脑镰入路行肿瘤切除,这样可避免双侧开颅,在不损伤对侧矢状窦旁桥静脉的情况下即可切除对侧肿瘤组织。

图3. 采用单侧直切口、经大脑镰入路并利用重力牵引脑组织行巨大镰旁脑膜瘤切除(上图)。侧卧位利用重力牵引使非优势半球远离中线(中图)。肿瘤位置通过重建模型图显示(下图)。
矢状窦旁桥静脉的位置应通过术前影像学检查仔细研究。如果肿瘤侧表面覆盖的桥静脉众多导致手术入路受阻,笔者会采用对侧经大脑镰入路显露肿瘤。
硬膜内手术步骤
镰旁脑膜瘤表面通常会覆盖一薄层正常脑皮质。由于颅内压力升高,开颅过程中钻孔的震动可能会损伤脑皮质,除非已行CSF引流降低颅内压。此外,颅高压失控将导致脑疝,尤其在暴露感觉运动区时会产生严重后果。

图4. 以矢状窦为基底,在硬膜外侧缘U形打开硬膜瓣,通过纵裂间隙抵达肿瘤部位。偶尔可以牺牲一些小的引流静脉,但千万不要损伤较大的引流静脉。如果硬膜剪开位置正好在矢状窦旁桥静脉引流入上矢状窦处,需要调整硬膜剪开位置以免影响静脉回流入窦。
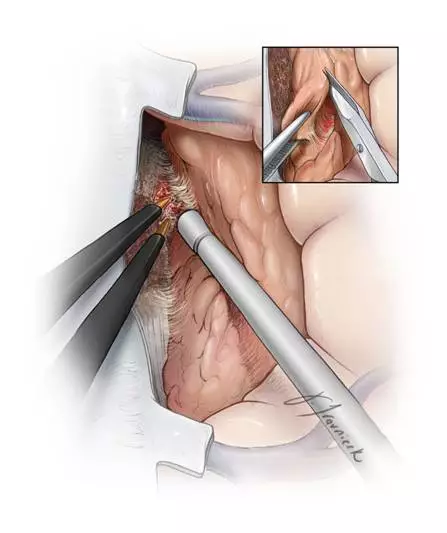
图5.大的肿瘤可侵犯凸面硬膜,可在硬膜瓣打开的过程中将其一并切除,但要注意保护毗邻桥静脉。首先断开肿瘤血供,接着逐渐切除瘤体,最后将瘤体自周边环绕的脑血管表面分离。
广泛分离纵裂蛛网膜、松解桥静脉后,在手术早期即可识别出沿大脑镰生长的肿瘤前后极及肿瘤深部毗邻的血管结构。腰大池引流对于这一步的操作安全至关重要。
首先,沿大脑镰将肿瘤供血动脉阻断(左图)。利用腰大池引流毋需早期减瘤即可使脑组织及肿瘤松弛,从而显露自大脑镰发出的肿瘤供血动脉。这一方法让快速阻断肿瘤基底部绝大部分血供成为可能。
由内向外逐步锐性切除肿瘤(右图),也可以使用CUSA替代。在切除过程中将肿瘤包膜逐渐拉入术腔同时维持肿瘤与软脑膜之间的手术界面。
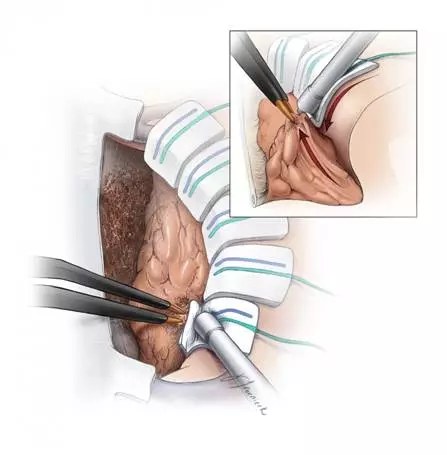
图6. 用双极沿肿瘤与软脑膜间的解剖间隙分离肿瘤包膜,双极电凝包膜可使之逐渐收缩。笔者会用棉片环形覆盖在脑表面,保持软脑膜与肿瘤间的界面。注意,该界面是沿肿瘤周边逐渐建立的,而不是在单一位置从浅至深建立。这样便可轻易移动瘤体(插图),以防出血时操作空间过于狭小。
如果软脑膜被侵犯,可利用脑棉“擦除”病变脑组织,并使之远离肿瘤,同时将肿瘤包膜推入术腔(插图)。将脑棉折叠“转动”着置入术腔深处建立一肿瘤与脑组织分隔的界面。重要的血管(胼周动脉及胼缘动脉)可能会与肿瘤粘连,予镜下锐性分离。每一根血管都必须仔细鉴别其是否肿瘤供血动脉,过路血管必须予以保留。
为了保护过路血管的完整性,宁可遗留一部分肿瘤在血管表面。为了避免血管痉挛,应尽量减少对血管的过度操作。
没有充分分离瘤周就过早的牵拉肿瘤下极将可能导致血管撕裂,造成严重后果。最后,检查术腔及病变硬脑膜边缘是否存在肿瘤残余。

图7.肿瘤切除后,用钩刀朝着上矢状窦方向切除肿瘤侵犯的大脑镰。如果上矢状窦未被肿瘤侵犯,必要时可牺牲下矢状窦。向大脑镰对侧扩张的肿瘤,须横断大脑镰建立对侧手术通道。也可以在开颅时将骨瓣向矢状窦对侧扩展,打开对侧的硬膜切除肿瘤。笔者更喜欢从单侧纵裂入路经大脑镰行对侧肿瘤切除术,这样能尽量避免对对侧矢状窦旁桥静脉造成损伤。
病例展示
以下展示的是一例体积巨大、双侧生长的镰旁脑膜瘤手术情况。

图8. 本病例通过单一右侧矢状窦旁入路经大脑镰切除双侧生长的镰旁脑膜瘤(第一排图)。利用大脑镰浅部的牵引缝线将上矢状窦向对侧移动(第二排图)。彻底阻断大脑镰右侧的肿瘤供血,部分切除肿瘤并仔细分离胼缘动脉(第三排图)。进一步切除肿瘤后暴露胼周动脉,经大脑镰切除对侧肿瘤并切除受累大脑镰(箭头)(第四排图)。
关颅
硬膜缺损采用预先留取的自体骨膜瓣缝合修补。悬吊硬膜用以预防硬膜外血肿及积液。
术后注意事项
术后须复查MRI。据病人耐受程度,激素缓慢减量。围手术期预防性使用抗癫痫药,若无癫痫发作,术后一周减量。术后短期内充分补液用以降低静脉血栓发生风险,特别是对于术中静脉窦或桥静脉被反复牵拉甚至被离端的患者。
点睛之笔
术前应行相关检查(包括MRI T2WI)预估大脑前动脉末端的分布情况。
尽可能减少桥静脉的牺牲。
术中处理大脑镰时,三叉神经-心脏反射可能造成心动过缓或停搏。
DOI: https://doi.org/10.18791/nsatlas.v4.ch02.3




