

前庭神经鞘瘤(Vestibular Schwannomas,VS)是起源于第八对颅神经的良性的肿瘤,占所有颅内肿瘤的8%,占桥小脑角(CPA)病变的90%。目前的治疗策略以显微手术切除为主。2009年,Suzuki等人提出了“神经束膜下(subperineurial)”切除的概念,让前庭神经鞘瘤的显微手术进入了一个新的阶段。今天我们分享一例由我科曹鹏教授团队近期经乙状窦后入路神经束膜下切除前庭神经鞘瘤的病例,同时进行文献回顾,与各位同道一同回溯一下前庭神经鞘瘤束膜下切除的“前世今生”。
01
病情介绍
患者女性,62岁,半月前无明显诱因出现头晕症状,既往左耳听力下降已有10余年。术前MRI检查结果提示:左侧桥小脑角区肿瘤延伸至内耳道,边界清晰,脑干略受压,增强扫描肿瘤呈均匀强化,左侧内听道扩大,肿瘤最大直径22mm。患者术前左耳感音神经性听力丧失(AAO-HNS D级)。(图1 )
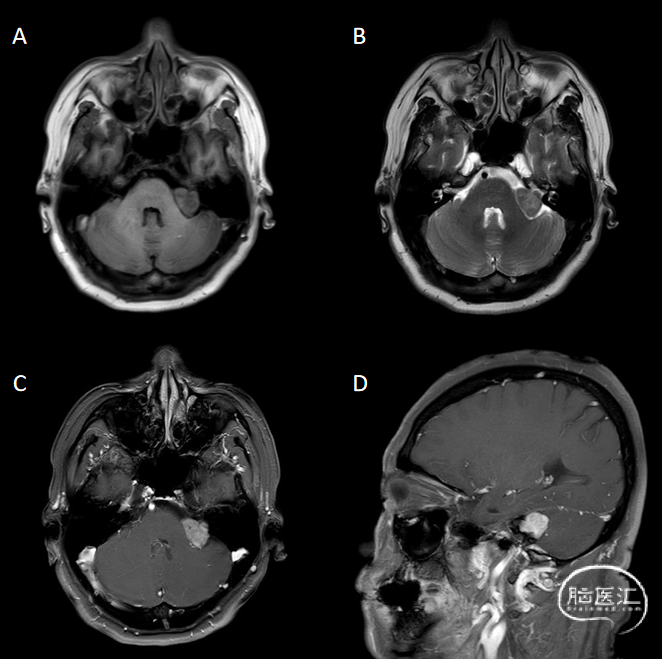
图1. 术前MRI。A、T1轴位,B、T2轴位,C、T1增强轴位,D、T1增强矢状位。
02
手术过程

视频1:手术视频
首先分离肿瘤表面蛛网膜,电生理刺激器确定肿瘤背侧无面神经后剪开肿瘤包膜,CUSA瘤内减容。在脑干端寻找神经束膜下平面,利用Rhoton 3剥离子沿神经束膜下平面向脑池段方向剥离肿瘤。磨钻磨除内耳道后壁,电生理再次确认面神经内耳道位置,小心分离并切除内耳道肿瘤,然后向脑池段汇合,最终完整切除肿瘤。面神经、蜗神经上的神经束膜保持完整。(图2)
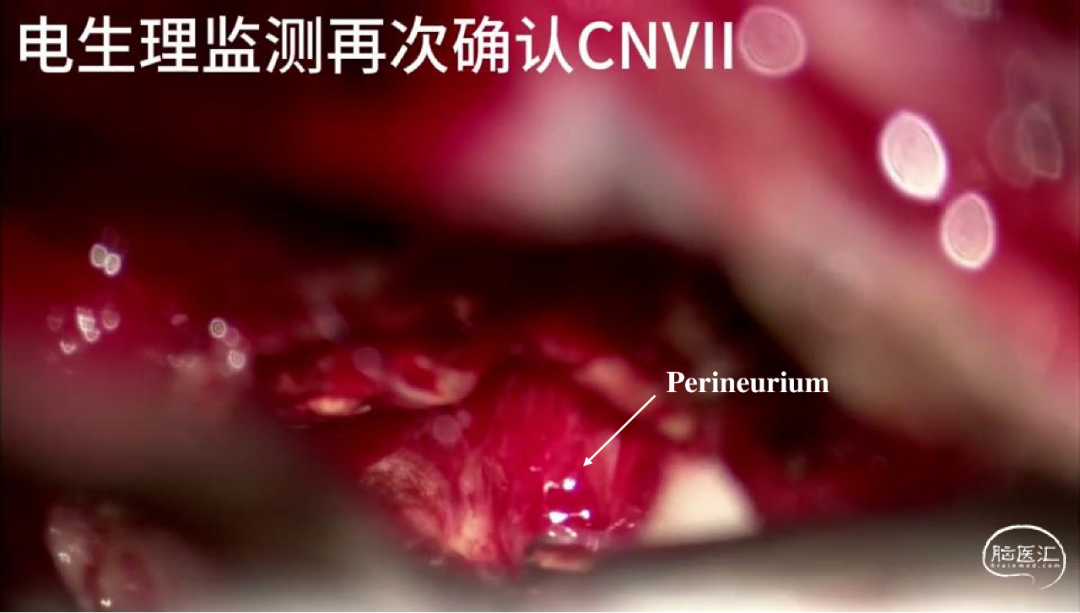
图2. 术中照片显示神经束膜结构。
术后复查头部MRI显示,肿瘤全部切除,听力检查与术前保持一致,术后两周面神经功能为House-Brackmann I级。(图3)
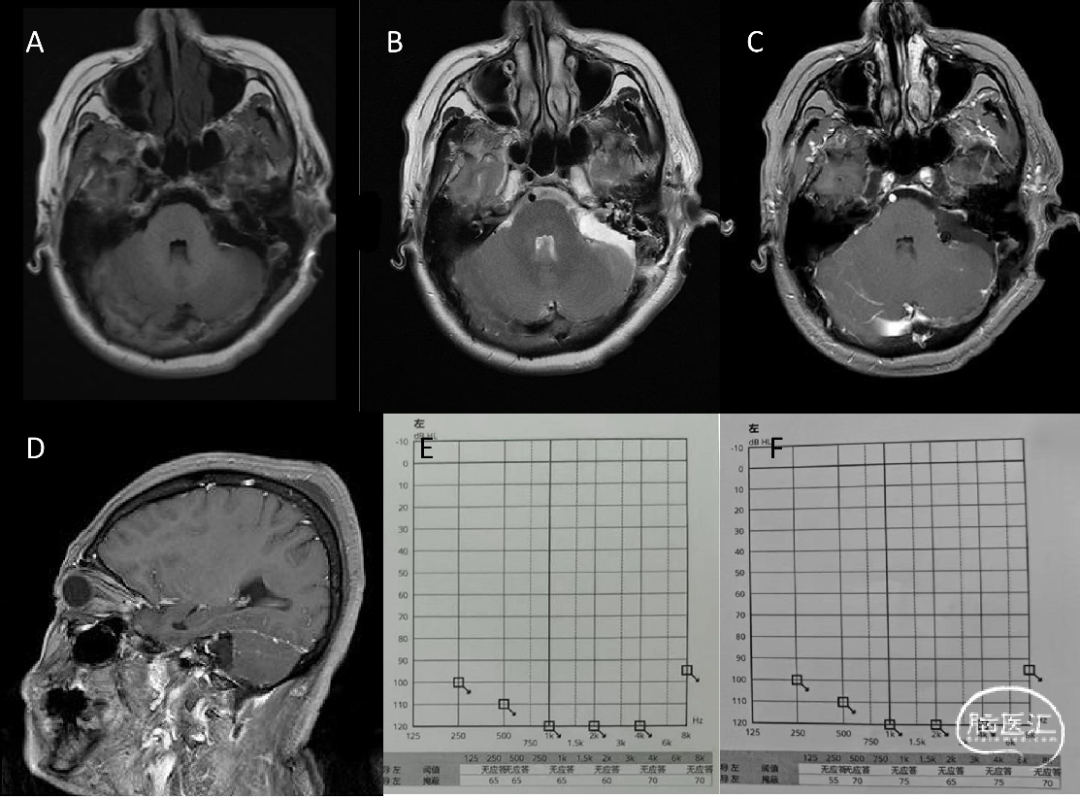
图3. 术后MRI。A、T1轴位,B、T2轴位,C、T1增强轴位,D、T1增强矢状位,E、术前听力检查,F、术后听力检查。
视频2:患者术后两周查体
03
文献回顾
前庭神经鞘瘤,其起源细胞围绕着第八颅神经的前庭分支。长期以来,它一直被不准确地称为听神经瘤(Acoustic Neuroma)。直到2019年在梅奥诊所举办的第八届前庭神经鞘瘤国际会议最终将其定名为“Vestibular Schwannoma.”[1]
在前庭神经鞘瘤手术发展的过程中,如何尽可能的切除肿瘤并保留神经功能始终是神经外科医生们探索的目标。1974年Yasargil与Fox合作发表论文[2],详细描述了通过蛛网膜间隙切除听神经瘤的方法。通过蛛网膜平面的分离可以明确肿瘤的界限,同时保留一层蛛网膜作为保护,可以避免神经损伤。此后通过蛛网膜下切除前庭神经鞘瘤成为被广泛认可的主流手术方式(图4)。2006年,Samii的划时代论文,报告了200名患者通过半坐位乙状窦后入路治疗VS听力及面神经功能保留情况,他仍然采取了经蛛网膜下切除肿瘤的方法,主张在切除肿瘤过程中通过瘤内减容,减少机械牵拉,采用半坐位,持续冲洗,减少出血进而减少双极电凝使用,双手分离操作,电生理监测等方式对神经进行保护。同时他采取先切除肿瘤核心,然后在蛛网膜平面环绕肿瘤进行切除的技术。如果没有肿瘤包膜,则会采用“洋葱皮”式的肿瘤切除技术,即从神经鞘瘤的内层到外层逐层切除,直至到达最外层并将其逐块切除。除了采用上述技术外,他还强调对于保留听力很重要的因素还包括应用3D神经导航、持续监测听觉诱发电位、通过在小脑延髓交界处尖端附有电极的牵开器直接记录脑干听觉诱发电位,以及使用内镜观察肿瘤最外侧部分。[3]可以说在蛛网膜下切除肿瘤的时期,Samii对手术的过程的精细把控几乎达到了巅峰。
然而,Samii的研究结果虽然较他之前的研究略有提升,但效果却并不显著。197名患者虽然有98.5%实现了面神经的解剖保留,但术后两周House-Brackmann分级I级和II级的患者比例仅为59%,排除术前面瘫的患者,该比例也仅为62%。有75.8%的患者耳蜗神经的解剖完整性得以保留,总体实用听力保留率为51%,小型肿瘤患者的实用听力保留率最高:T1级患者为57%,之后逐渐下降,T2级患者为54%,T3a级患者为42%,T3b级患者为34%。
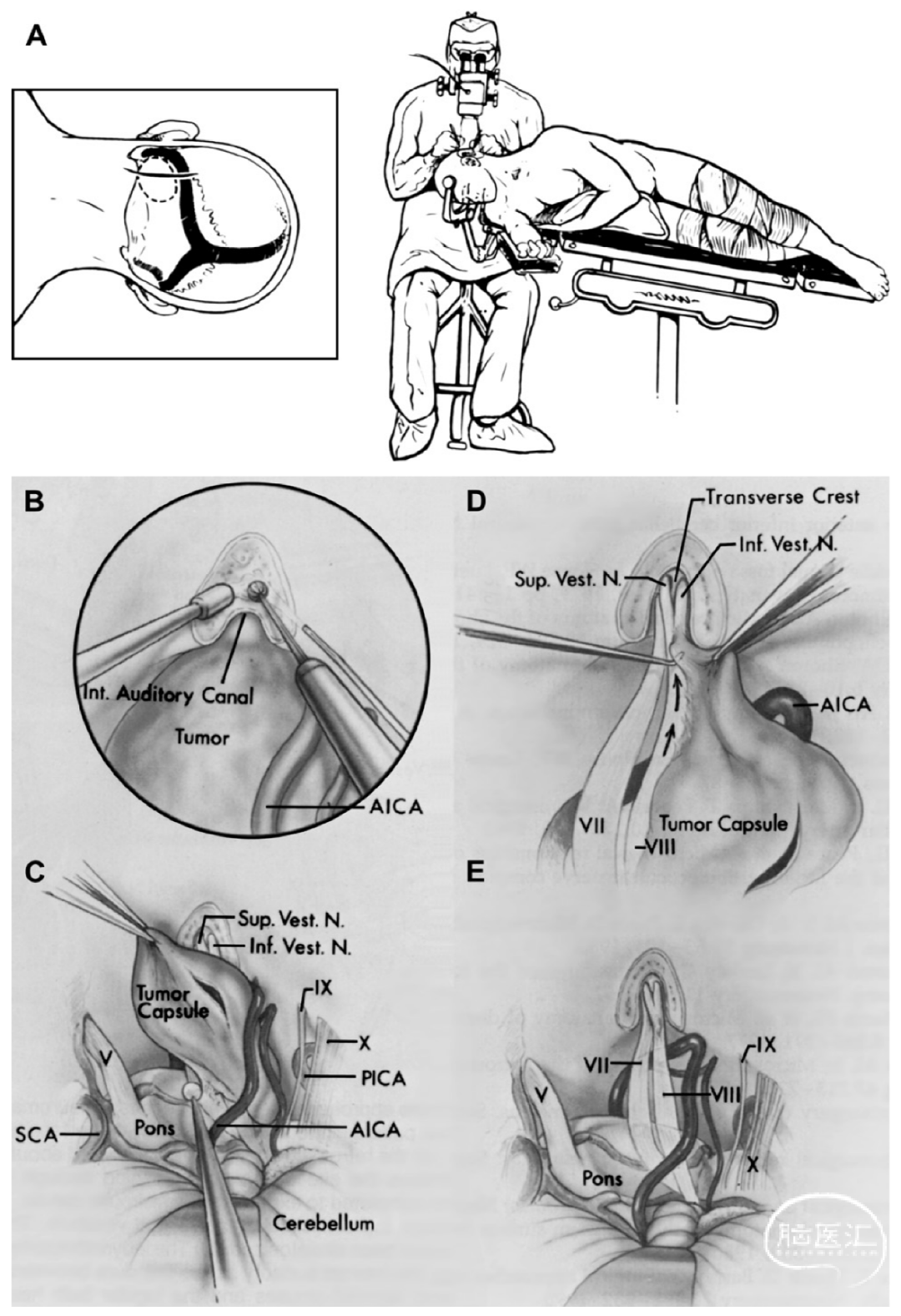
图4. 乙状窦后入路蛛网膜平面除术前庭神经鞘瘤手术方式示例图,引自Rhoton等人的文章。[4]
2009年,Suzuki等人发表了《Histological considerations of the cleavage plane for preservation of facial and cochlear nerve functions in vestibular schwannoma surgery》,率先从组织学的角度分析了前庭神经鞘瘤包膜以及肿瘤与神经的界面,确定了一个理想的手术平面(神经束膜下平面),从而最大程度的切除肿瘤并保留神经功能。
Suzuki等人通过组织学染色证实,在肿瘤表面,存在一层连续的薄结缔组织层,在这层薄结缔组织下方,有一些退化的前庭神经纤维,外侧的这层薄结缔组织层被认为是前庭神经的神经束膜(Perineurium)。VS的部分肿瘤包膜实际上就是残留的前庭神经组织本身,由神经束膜和其下方的神经纤维混合组成。在分析连同蜗神经一并完整切除的肿瘤标本中,作者发现,在蜗神经和肿瘤之间存在一层由蜗神经和前庭神经的神经束膜构成的结缔组织层,这层组织清晰地将神经纤维与肿瘤组织分隔开来。这种由双层束膜及部分残留的前庭神经纤维组成的较为密实的结构可以有效的保护蜗神经,这为神经束膜下切除肿瘤奠定了结构基础。(图5)
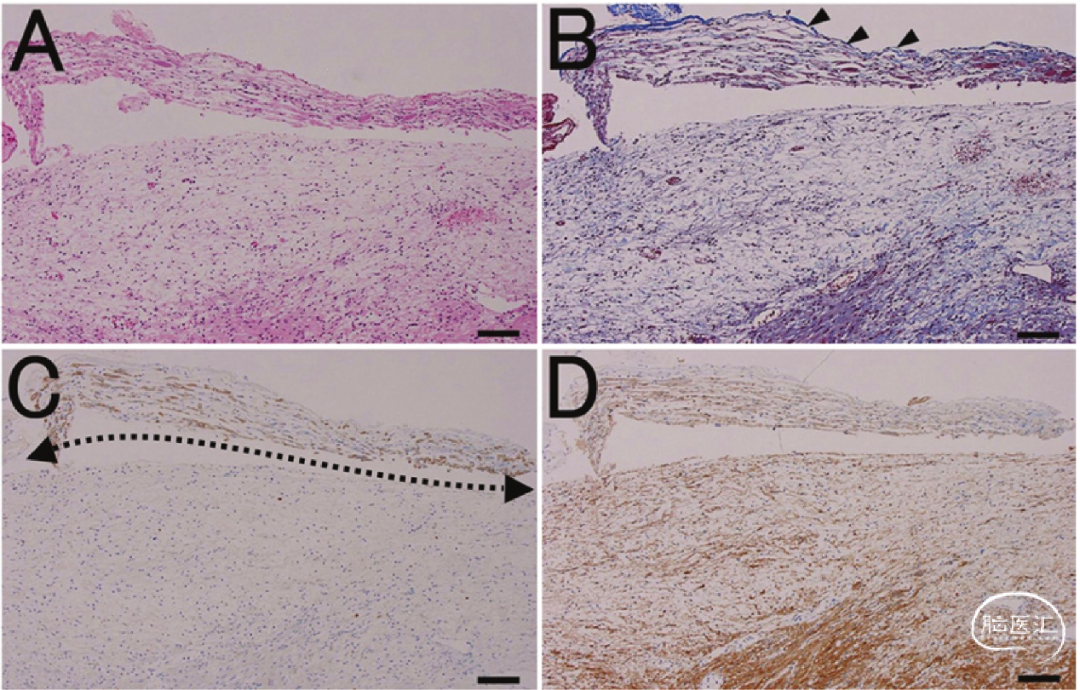
图5. 前庭神经鞘瘤游离面的显微照片,引自Suzuki等人研究[5]。A:苏木精-伊红染色(H&E染色)。B:马松三色染色显示肿瘤表面的薄结缔组织(箭头所示)。C:髓鞘碱性蛋白(MBP)免疫染色,在苏木精复染切片中可见棕色的神经纤维(虚线箭头表示理想的解剖平面)。D:S100蛋白染色的前庭神经鞘瘤组织。在苏木精复染切片中,神经纤维和肿瘤性施万细胞呈棕色。
在手术中,肿瘤包膜与这些神经纤维确实存在广泛的粘连,从病理学上分析,即前庭神经的神经束膜与蜗神经、面神经的神经束膜之间存在粘连,这种情况在内耳道孔周围区域尤为明显。在该区域面神经或蜗神经纤维常常会因肿瘤而扩张和变扁。在这些区域,由于神经纤维极其脆弱,直接在束膜间操作神经纤维对于功能保留来说风险极大。选择进行神经束膜下剥离,有时甚至保留一薄层肿瘤组织,可以避免直接操作这些神经纤维,进而保留神经功能(图6)。
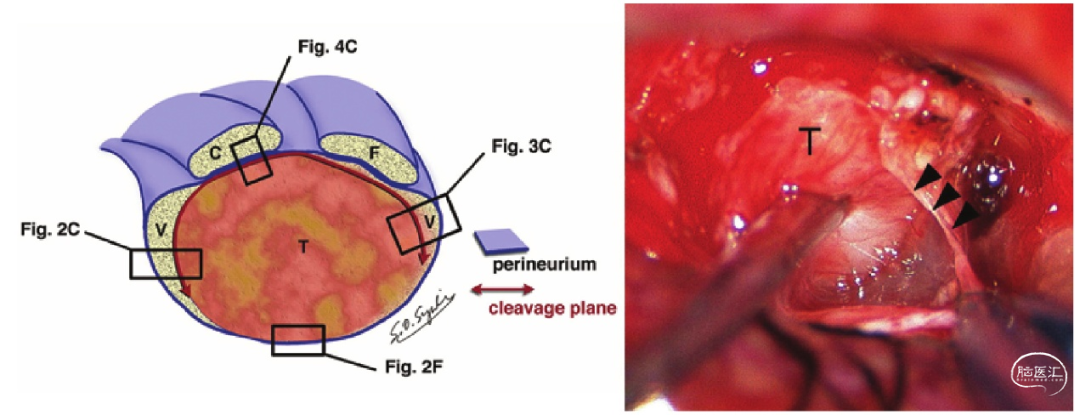
图6. 左图:前庭神经束膜模式图及术中照片,引自Suzuki等人研究[5]。前庭神经鞘瘤手术中为保留面神经(F)和蜗神经(C)进行囊下剥离的示意图。蜗神经和面神经在肿瘤边界处有一层结缔组织。在这层结缔组织下方,可见一层前庭神经(V)纤维,或前庭神经纤维与肿瘤细胞的混合层,这两者都可作为保留面神经和蜗神经功能的解剖平面。右图:前庭神经鞘瘤(T)的术中照片以及囊下剥离平面(箭头指示肿瘤包膜,即一层薄结缔组织和前庭神经纤维)。
该研究术后结果显示,直径小于2厘米的肿瘤,全切除或近全切除率达到了94.9%(79例中有75例);直径在2至4厘米的肿瘤,这一比例为86.0%(150例中有129例);直径大于4厘米的肿瘤,全切除或近全切除率为77.8%(45例中有35例)。术后1年面神经功能良好(House-Brackmann Grades I级和II级)的比例为95.5%。当肿瘤直径小于2厘米时,所有病例(79例中的79例)都实现了解剖学保留,术后1年98.6%(74例中的73例)的患者面神经功能良好。在112例患者术前肿瘤侧具有有效听力(Gardner-Robertson Classes I级和II级)中,52.7%(112例中的59例)的患者保留了有效听力。当肿瘤直径小于2厘米时,64.2%(53例中的34例)的患者保留了有效听力[5]。对于直径大于2厘米的VS(对应New Hannover Classification Class T3b级肿瘤到达脑干)效果(42.4%)也明显优于Samii等人的研究(34%)[3]。在后续随访中,(平均随访期为100.1个月,范围为2至332个月)在274名单侧VS患者中,有5例(占1.8%)因肿瘤复发需要再次进行切除手术。在这5例患者中,有3例在首次手术时进行了近全切除,2例进行了次全切除或部分切除。以上结果显示,束膜下切除技术在小于2cm的肿瘤切除中对神经的保护是十分显著的,即使在体积较大的VS切除中也同样具有优势。
尽管Suzuki等人的研究结果具有开创性,但此后近10年却鲜进一步的研究报道。直到2019年,Jyung和James K. Liu等人连续发布三篇听神经瘤手术视频文章,分别经经迷路入路和乙状窦后入路详细展示了神经束膜的结构以及束膜下切除的手术过程。

视频3:Translabyrinthine Approach for Resection of Large Cystic Acoustic Neuroma: Operative Video and Technical Nuances of Subperineural Dissection for Facial Nerve Preservation 手术视频
对于手术入路的选择,Jyung和James K. Liu等人是根据肿瘤大小,患者听力保留情况,肿瘤是否向内听道有限延伸所决定。迷路入路的暴露范围更大,不需要小脑过度回缩,但势必会造成听力损伤,因此对于肿瘤较大压迫脑干,且听力完全丧失的患者较为合适。而对于较小的肿瘤,向内耳道的延伸和脑干压迫不是很明显,且保留一定听力的患者,更适用于乙状窦后入路。该入路对听力可以较好的保留。

视频4:Retrosigmoid Transmeatal Approach for Resection of Acoustic Neuroma: Operative Video and Technical Nuances of Subperineural Dissection for Facial Nerve Preservation 手术视频
在分离肿瘤的过程中,作者采用了“推开(push-away)” 技术,即Rhoton 3号圆盘剥离器的尖端置于肿瘤顶部,而圆盘的扁平部分则将神经束膜推开。在分离肿瘤与神经束膜之间的粘连部分时,作者使用McElveen刀和显微剪刀进行锐性分离。对于与神经束膜层紧密粘连的肿瘤部分,作者认为可以在束膜下修剪掉,但要留下一小片肿瘤残留,以避免损伤面神经。

视频5:Retrosigmoid approach for giant cystic vestibular schwannoma: subperineural dissection technique for facial nerve preservation 手术视频
在整个手术过程中,面神经是不显露出来的,保护在神经束膜之后,可以用神经电刺激来确定面神经的位置。将神经束膜保留在脑干和神经表面,利用神经束膜作为缓冲(buffer),这样既可以使肿瘤切除体积最大化,尽量减少肿瘤残留,同时很好的保护了神经。视频中,作者强调神经束膜包裹肿瘤,其外观与蛛网膜类似[6,7]。由此我们猜想,既往很多神经外科医生进行的蛛网膜下前庭神经鞘瘤的切除其实是神经束膜下切除,只是当时没有被认识到。(图7)
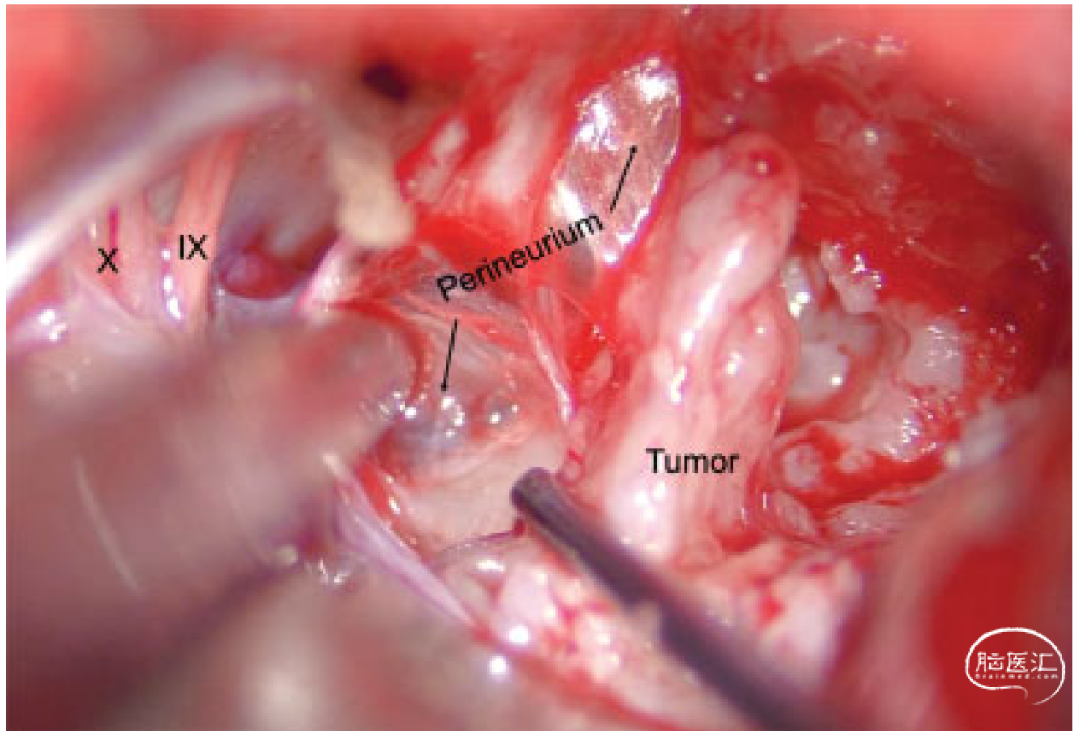
图7. 术中照片展示了前庭神经束膜与肿瘤之间的束膜下解剖平面,引自James K. Liu等人的手术录像照片[6]。
随后,Nakajima及Froelich等人也分别发表文章,通过典型案例详细描述了神经束膜下切除前庭神经鞘瘤的要点,强调了束膜下解剖平面利用硬膜样膜、蛛网膜、前庭神经束膜的叠加结构,形成清晰的无血管界面,避免直接暴露面神经与蜗神经,Froelich所在医院更将该技术主要应用于Koos Ⅲ、Ⅳ级VS的切除中[8,9]。
2021年,Youssef和Lawton等人发表包含10名患者的队列研究,进一步介绍并评估了束膜下切除技术。作者首先从肿瘤的内下部分开始,使用显微剪刀和锐角显微剥离器在肿瘤和前庭神经之间锐性分离出一个层面,并识别出耳蜗神经。在已经分离出的肿瘤和前庭神经束之间的层面上,从内侧向外侧进行分离。以前庭神经作为隔离层,保护其下方的耳蜗神经和面神经。然后磨除内耳道后壁,识别利用电生理出不同的神经,锐性切断远端的肿瘤神经,使肿瘤脱离,同时保留未受侵犯的前庭神经。接着将肿瘤向内侧卷离,同时使用其他完整的前庭神经束作为耳蜗神经和面神经的保护屏障。通过这种方式实现了肿瘤的大体全切除。
该研究中所选病例肿瘤均小于2cm,其中3例Koos分级为Ⅲ级的肿瘤和7例分级为Ⅱ级的肿瘤。9名患者术前听力AAO-HNS分级为A级,1名患者为B级。所有患者均实现了肿瘤全切除。所有病例中面神经和蜗神经在解剖学上均得以保留。术后,7名患者(70%)的听力仍保持在的A级或B级。10名患者术后面神经功能均维持在 House-Brackmann(HB)分级1级[10]。结果表明,在小于2cm的肿瘤切除中,该技术通过保留前庭神经,尽量减少对面神经和蜗神经的操作,显著改善了手术效果,尤其是在听力保留方面。但文中并未提及该研究的复发率情况。
文中还提出肿瘤与前庭神经、面神经的位置构型的不同也对手术产生影响。当神经被肿瘤分隔开,蜗神经在肿瘤下方,面神经在肿瘤上方(图8),这种情况下,对于保留前庭神经和听力是一种挑战。
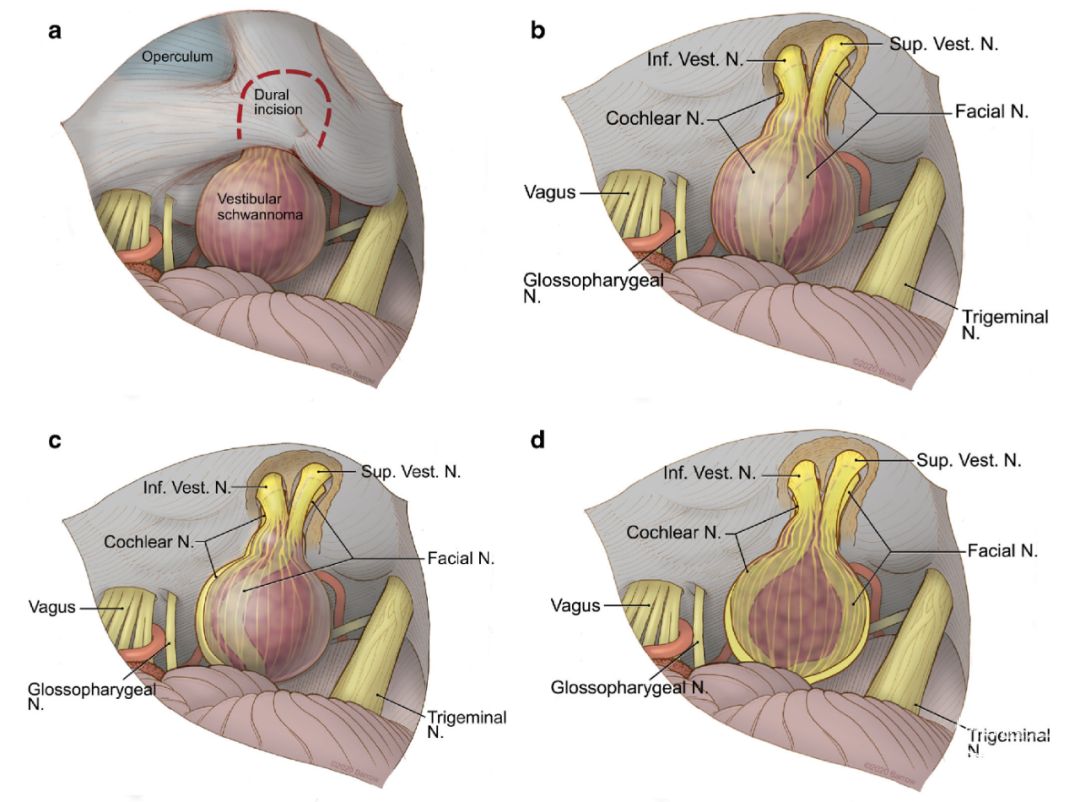
图8. 前庭神经鞘瘤周围的颅神经构型。(A)从乙状窦后入路切除前庭神经鞘瘤的手术视野示意图。(B)1型——面神经向前移位。(C)2型——面神经向下移位。(D)3型——面神经向上移位,且被肿瘤与蜗神经分隔开。
作者还在文中还对比了放射治疗和显微手术的效果,提到美国神经外科医师协会指南以及其他报告都表明,放射治疗10年以上的听力保留概率处于中等偏低水平(25%至50%)。而显微手术的术后即刻的听力保留率在35%至72%之间,而且极少有长期听力下降的报道。说明显微外科手术较放射治疗对于听力的保留有更好的长期预后。
2022年,空军军医大学附属唐都医院屈延团队对此也进行了探索和尝试。他们报道了124位接受神经束膜下切除VS患者的疗效研究。肿瘤全切除(GTR)率为83.9%,20例患者实现了肿瘤次全切除(STR)。术后121例(97.6%)面神经实现完全解剖保留,96例患者(77.4%)House-Brackmann(HB)评分为I-II级(功能良好)。在35例术前有实用听力的患者中,15例(42.9%)在术后6个月仍有实用听力[11]。
专家点评
赖杰宇教授:
面听神经的保护一直是前庭神经鞘瘤切除的难点。由于前庭神经鞘瘤的复发与肿瘤残余大小息息相关,因此最大化地切除肿瘤和最小的神经损伤一直是我们努力的目标。二者在神经束膜平面似乎达到一个平衡,使得手术治疗收益最大化。该患者肿瘤体积较小,向内耳道入侵不是特别明显,虽然术前左耳听力丧失,但即使是 AAO – HNS D级的患者也可能在术后出现听力改善。因此依然需要努力保护面听神经的完整性。术者选择神经束膜下切除,减少了对神经的刺激,同时达到了肿瘤全切的目的,期望术后患者听力能有所恢复。同样,选择乙状窦后入路也是基于上述考虑,因为迷路入路不可避免地破坏内耳结构。根据术后检查及随访的结果,手术基本达到了预期的效果。
梁国标教授:
在蛛网膜层面切除VS时期,神经外科医生通过瘤内减容,减少机械牵拉,采用半坐位,持续冲洗,减少出血进而减少双极电凝使用以及神经电生理监测等多种方式的综合运用,以求更好的保护面听神经的功能。而神经束膜下切除技术是在此基础上向前又迈进了一步。该技术巧妙地利用了前庭神经束膜以及残留的前庭神经纤维这些结缔组织作为缓冲,在不降低全切/次全切率的情况下,进一步保护了面听神经。使VS显微手术进入了全新的时代。手术中有两点需要注意,一是沿神经束膜切开,从内听道口处仔细地锐性分离界面。二是采用由内到外分离,远端与近端分块切除,最终会师在面听神经结合处,始终做到无张力分离。这两点对面听神经的保护至关重要。从目前的资料看,该技术对面听神经功能的保护,短期内有良好效果。即使在较大的肿瘤切除中,也能提高听力的保留率。目前,神经束膜下切除仍然是一个较为新的技术,需要我们更多的去实践训练,未来仍需要对更大样本量的患者群体开展研究,以确定这一策略的长期功能预后情况以及对肿瘤复发的控制效果。
参考文献:
作者简介
曹源 主治医师
北部战区总医院
北部战区总医院神经外科主治医师,医学博士,博士后,长期致力于脑肿瘤、神经损伤修复、神经干细胞发育等神经系统相关疾病的临床及基础研究。
曹鹏 副主任医师
北部战区总医院
北部战区总医院神经外科肿瘤病区副主任医师,医学博士博士后,芬兰赫尔辛基大学中心医院访问学者,师从全国著名神经外科专家北部战区总医院神经外科梁国标教授,任中国医科大学,大连医科大学,锦州医科大学硕士研究生导师,辽宁省医学会神经外科分会常委,获辽宁省科技进步二等奖1项,主持多项国家省部级课题,累计发表SCI论文15篇、单篇最高影响因子13.3分,累积影响因子81.1分,核心期刊论文数十篇,获手术器械国家专利8项,主编神经外科专著多部。
点评专家
赖杰宇 主任医师
北部战区总医院
北部战区总医院神经外科主任医师。主要从事脑肿瘤疾病的诊断、治疗和研究工作。全军神经外科分会委员,中国研究型医院神经微创学会委员,中国医学会神经神经损伤分会常委,中华医学会辽宁省神经外科分会委员。
梁国标 主任医师
北部战区总医院
● 北部战区总医院神经外科主任,主任医师
● 全军神经医学研究所所长,中华医学会辽宁省神经外科分会候任主委、辽宁省神经介入学会主任委员,辽宁省神经介入组组长,中国研究型医院学会神经微侵袭专业委员会主任委员、世界华人神经外科协会委员、中国医师协会神经外科医师分会委员、中国医师协会介入医师分会委员、中国医师协会脑血管病专家委员会委员、中华医学会神经外科学分会脑血管病学组副主任委员、全军神经外科学专业委员会常务委员
● 担任《Neurosurgery》和《Neurology India》审稿专家,《中华神经外科杂志》《中华实验外科杂志》《中国临床神经外科杂志》《创伤外科杂志》《中国微侵袭神经外科杂志》《临床误诊误治》《解放军医药杂志》编委等职
● 先后荣获辽宁“兴辽英才”计划科技创新领军人才,沈阳市杰出医师奖,沈阳市第七届优秀专家,军区科技发展创新人才等荣誉称号。承担国家十一五、十二五科技支撑计划子课题各1项、国家自然科学基金2项、辽宁省重点项目指导计划1项、辽宁省科技攻关课题1项,辽宁科技创新领军人才项目课题1项,辽宁省博士科研启动基金计划项目课题1项
● 以第一完成人获军队医疗成果二等奖一项,以第一完成人获辽宁省科技进步一等奖一项,辽宁省科技进步二等奖两项,军队及辽宁省省科技进步三等奖6项,享受军队优秀专业技术人才岗位津贴
● 发表各类核心期刊200余篇,SCI文章80余篇

声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。











